
녹십자랩셀이 10여 년간의 NK세포치료제 연구를 바탕으로 3년 내 미국에서 신약을 출시하겠다는 청사진을 내놨다. 녹십자랩셀은 제대혈 유래 NK세포치료제 'AB101'과 항체치료제 리툭산을 혈액암 환자에게 병용하는 임상 1/2상 시험계획(IND)을 이르면 이달 중 미국 식품의약국(FDA)에 제출할 예정이다.
▶T세포와 달리 동종치료제 가능
황유경 녹십자랩셀 연구소장(사진)은 "임상시험을 성공적으로 마치는 대로 조건부 허가를 받을 수 있게 FDA와 협의했다"며 "국내에서 임상 2상을 진행 중인 간암 치료제보다 더 빨리 허가받을 수 있을 것"이라고 3일 말했다.
그는 국내의 대표적인 NK세포 연구자로 꼽힌다. 1990년 목암연구소에 입사해 아주대 의대에서 면역학 박사학위를 받았다. 미국 인디애나대에서 박사 후 연구원 과정을 마쳤다. 2009년 회사로 돌아와 본격적으로 NK세포치료제 개발을 이끌었다.
NK세포는 인간이 태어날 때부터 가지고 있는 면역세포의 일종이다. 심각한 면역 거부 반응 때문에 환자 자신에게만 투여할 수 있는 T세포와 달리 NK세포는 모든 환자에게 투여할 수 있다. 그러나 NK세포의 효율적 배양이 2000년대 들어서야 가능해지면서 바이오 업계에서 이를 활용한 연구개발이 활발히 이뤄지고 있다. 황 소장은 "NK세포가 안전할 뿐 아니라 T세포와 맞먹는 항암 효과를 가지고 있다는 연구가 많이 나오면서 업계의 주목을 끌고 있다"고 했다.
녹십자랩셀은 대량 배양 기술과 장기간 보존 및 운송이 가능한 동결 보존 기술을 자체 개발했다. 그는 "NK세포를 배양하려면 먹이세포를 써야 하는데 우리는 이를 자체 개발한 소수 기업 중 하나"라며 "고순도의 NK세포를 1000억 개 이상 만들 수 있다"고 했다.
▶항체치료제 병용 집중
올해 안에 미국에서 임상을 시작할 AB101은 제대혈에서 추출한 NK세포를 대량 배양한 물질이다. 제대혈에서는 말초혈액보다 상대적으로 품질이 일정한 NK세포를 얻을 수 있어 동종 치료제 개발이 유리하다.
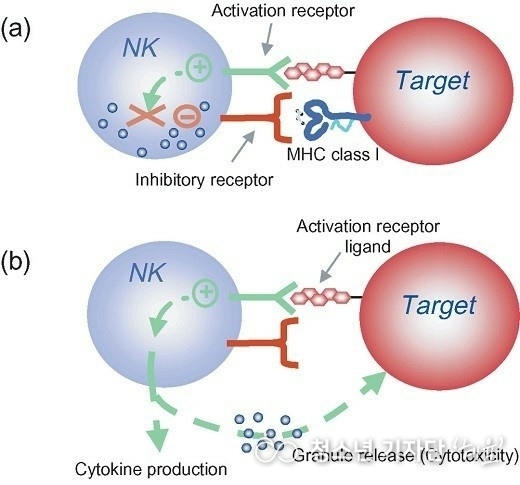
녹십자랩셀은 항체치료제와 병용할 수 있는 NK세포치료제를 적극 개발하고 있다. 항체와 NK세포를 붙게 하는 물질인 'CD16'이 잘 발현되는 NK세포를 배양하는 기술을 이용해서다. 황 소장은 "경쟁사들은 유전자 조작을 통해 NK세포에 CD16이 발현시키는데 우리는 이보다 효율적인 배양 기술을 보유하고 있다"고 했다.
AB101 개발은 지난해 3월 설립된 미국 자회사 아티바가 전담한다. 아티바는 미국, 유럽 등 선진국 시장에서 임상 개발을 맡고 있다. 녹십자랩셀은 지난해 11월 AB101을 아티바에 기술이전했다. 최고경영자(CEO), 최고기술책임자(CTO) 등을 벨리쿰, 주노, 페이트 등 미국의 주요 세포치료제 업체에서 영입했다. 그는 "우리는 연구에 집중하고 아티바는 임상 개발 경험이 풍부한 인력을 주축으로 사업을 진행할 것"이라고 했다.
녹십자랩셀은 앱클론(한국), 펠던(캐나다), 모포시스(독일), 유니버설 셀(미국) 등 여러 기업과 폭넓은 협력을 통해 NK세포치료제 후보물질(파이프라인)을 확대하고 있다. 유전자 편집 NK세포치료제, CAR-NK세포치료제, 줄기세포 유래 NK세포치료제 등 혁신 기술을 접목해 약효를 높이고 있다. 황 소장은 "AB101에 이어 차례로 미국에서 임상을 시작할 것"이라고 했다.
신종 코로나바이러스 감염증(코로나19) 치료제 임상도 국내와 미국에서 이르면 연말에 시작한다. 황 소장은 "미국 등 해외에서 임상을 진행하자는 요청이 오고 있다"고 했다.





